本文描述了与生物药物产品的冻干相关的挑战。采用质量源于设计(QbD)方法和SP Line of Sight™技术套件, 提供了一个丰富的数据环境,其中许多挑战可以被克服。Line of Sight™包含全套的设备、技术和PAT工具,可以简化冻干制剂从早期开发到生产放大,加速商业化生产。从事于生物制剂的公司需要靠得住的流程和经过验证的数据来交付成功的产品。

生物药物在治疗许多改变生活的疾病方面显示出了巨大的前景,甚至包括一些曾经被认为无法治愈的疾病。然而,由于生物材料的敏感性,它需要专门的开发和制造工艺。冻干的稳定性对保持产品的生物活性、结构完整性和质量均一性是非常有吸引力的,而所有这些都是产品成功的关键。
1、背景介绍
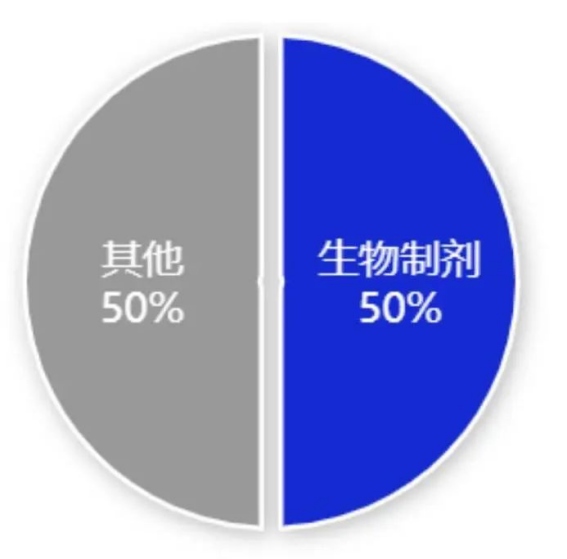
临床管线中50%的药物由生物制剂组成。大的生物分子,通常是蛋白质或抗体,给药需要不同于标准固体或半固体药物制剂的制造能力。生物药物和抗体-偶联药物(ADCs)不仅生产成本很高,而且有些还不如其他制剂或分子稳定。在储存和运输过程中保存它们的活性也是非常困难的。此外,产品温度监测的重要性不能低估,特别是当工艺转移到具有无菌环境的较大设备时,应将测量产品温度的解决方案视为开发策略的一部分。
为了克服这些要求并延长保质期,冷冻干燥是相对较好的方式。冻干过程将产品的温度降低到冰点以下,然后使用受控真空升华除去水或其他溶剂。至少41%的生物药品和几乎所有ADCs都是冷冻干燥的,以保持其物理结构。ADCs的冻干可保障在储存和运输过程中连接“ payload”与antibody的 linker的稳定性。冻干生物制剂可以快速复水,同时保持其生物活性。
冷冻干燥过程中的每一部分都对产品的质量和完整性有很大的影响。随着技术的进步和更多工具的运用,人们可以更好地理解如何测量和记录影响最终产品的参数,从而对产品本身有更多的了解。美国FDA和其他监管机构强烈建议采用质量设计(QbD)方法,以确保产品性能。FDA早在2011年1月发布的过程验证指南中指出:“企业需要继续从获得的知识中受益,并通过调整在整个过程生命周期中不断改进,使得生产问题的根源迅速得到纠正”。这种从试错方法到基于科学的冻干过程方法的转变,为这些生物药物的体内产品性能提供了信心。
2、QbD方法—优化冻干生物制剂
生物药物数量的增加往往服务于小目标人群,这导致对开发人员和制造商的更大要求,以提高产量和更好的产品质量来提高效率。批次内部和批次之间的一致性是基于从物理外观和结构完整性到生物活性等几个特性的整体质量参数。注射用药物在生产过程中也要求高度无菌。在无菌环境中,通过加强对冷冻干燥过程的控制,可以缩短开发时间,提高稳定性和质量。
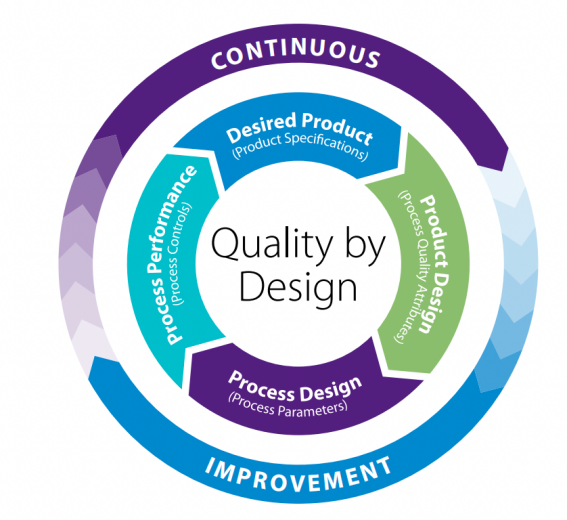
图1:质量源于设计(QbD)方法
要解决这些挑战,首先要在产品生命周期的早期对其有一个很好的理解。从一开始就更好地开发冷冻干燥工艺以实现较理想的的大规模商业化,并从长远来看降低经济负担。然而,即使有了这些知识,扩大规模对生物药物制造商来说仍然是一个持续的挑战。冻干设备的性能和操作在开发和生产规模之间可能存在差异,这导致在每个阶段对冻干参数进行耗时和昂贵的重新优化,以实现产品的成功冻干。
药品生产QbD方法的一部分是利用过程分析技术(PAT)改进冷冻干燥工艺,以便能够很好地定义关键工艺参数,并及时了解和监测其对产品质量的影响。要特别注意这些参数将创造一个优化的设计操作空间,从而降低成本。
3、理解设计空间
作为QbD方法的一部分,一种系统的开发方法从预定义的目标开始应用,并强调对产品和过程的理解。这得到了科学知识和质量风险管理的支持,以建立一个设计空间和已定义的操作变量集,以保持批处理的一致性(图2)。这些参数以图形方式表示为多维点,以定义维护批处理一致性所需的操作变量集。 在设计空间(操作空间)内的操作将使产品达到预定义的质量。
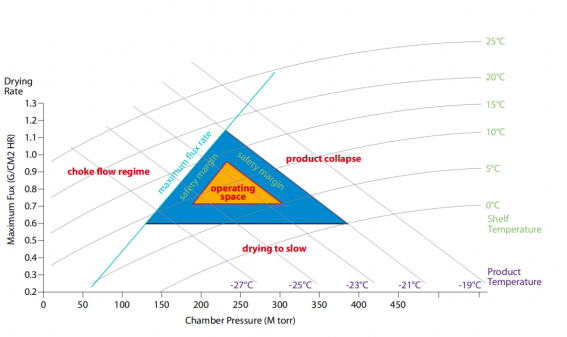
图2:冻干工艺的设计空间
设计空间的简化描述——设备能力极限和产品知识的多维表示
4、一套工具—用于生物制药冻干生产放大
Line of Sight™

认识到生产放大的内在挑战和对改善生物药物开发和制造结果的愿望,ATS SP创建了Line of Sight (LoS)。
LoS是一套工具——技术和设备,可用于开发和生产的每个阶段,以提高冻干过程控制、效率、质量和一致性。
这套技术和PAT被内置到小型冷冻干燥机中,通过大型商业化生产冻干机为研究和生产冻干专业人员提供了一种清晰的,由实时数据支持的流程方法。这种方法还使得一种设备的技术和方法可以复制并直接与另一种设备进行比较。
LoS的工具包括:
● Lyoccapsule™微型冷冻干燥机:7瓶开发-适用于昂贵的药物和早期配方或工艺开发;
● LyoStar™4.0研发型冷冻干燥机:冻干工艺开发和优化的“主力”及”优选工具“;
● LyoConstellation™系列大型冷冻干燥机:不仅可以进行冻干工艺开发,还可以提供无菌GMP操作。
所有这些冻干机都配备PAT工具,包括:
● ControLyo®技术用于晶核控制 ;
● SMART™技术用于加速初级干燥开发和优化;
● LyoFlux* TDLAS蒸汽质量流量传感器,非侵入式实时监测关键产品和过程数据;
● 无线Tempris*传感器用于产品温度测量;
5、提高冻干工艺效率
冻干效率依赖于获得具有较少浪费(材料、能量、时间、金钱)的高质量产品。创建设计空间的预定义的操作变量集决定了过程效率。拥有更大的设计空间,或要工作的参数,可以增加重复执行成功工艺的概率,即使面对潜在的问题,包括计划外的过程偏差。LoS可以通过理解流程参数如何影响关键的产品属性来扩展特定目标的设计空间。
6、一次干燥工艺优化工具
SMART冷冻干燥技术
SMART冷冻干燥技术是一项PAT工具,使用压力温度测量(MTM)技术来确定冻干饼的阻力和升华界面的产品温度。随着AutoMTM允许研究人员在报告关键工艺和产品参数时运行自己的预定周期。SMART技术已被证明可以节省大量宝贵的开发时间,并提供过程相关的关键产品数据。
在与一家大型制药公司和两家生物技术公司的比较研究中,SMART技术被用于开发对应配方的优化周期。所有三个实验室报告表明,他们在不到三个月的时间内收回了投资,平均开发时间缩短了62天。此外,科学家通常能够在单次实验运行后产生一个优化的工艺,这样就有时间进行进一步的实验来测试工艺极限。这些结果还意味着,一种配方可以比目前的时间框架提前几个月进入中试生产阶段。
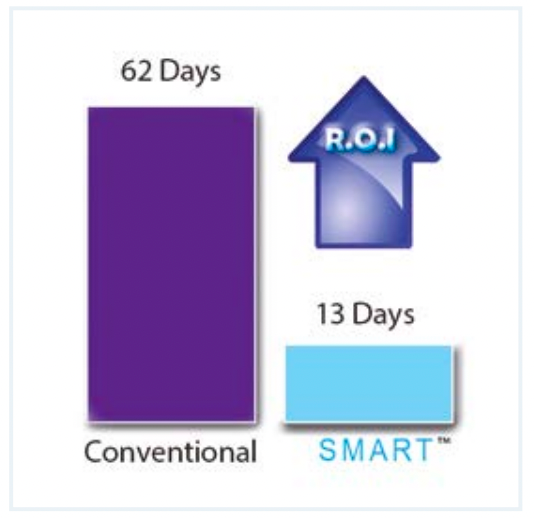
图3:投资回报(ROI)示例:使用传统方法VS Smart 技术开发工艺
7、准确测量蒸汽质量流量
PAT工具——TDLAS
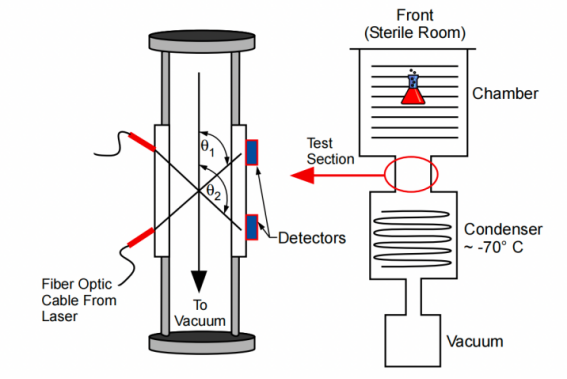
图4:应用于Lyostar 冻干机上的TDLAS技术
通过LoS技术套件中的另一个PAT工具(TDLAS)可以对冻干过程和放大进行有效实时监测和测量。LyoFlux传感器使用可调谐二极管激光吸收光谱(TDLAS)技术来测量水蒸气浓度和流速,由此可以得出特定配方的升华界面温度。LyoFlux可以在短短三个实验中计算特定产品的工艺设计空间参数,而传统上至少需要5次或6次运行。使用LyoFlux技术,可以通过一次运行获得最大升华速率来确定设备性能。一旦该设备的设备能力建立,可以确定用于产品的小瓶的传热系数Kv。同样,LyoFlux可以通过改变腔室压力和监测各自压力设定点的升华速率,在一次测试中执行多个实验。LyoFlux还可以确定在小瓶中冷冻干燥过程中的饼阻力。这简化了生产冷冻干燥机的使用,并尽可能大限度地减少了进行多组实验所需的停机时间,从而获得产品属性和设备性能数据,以便进一步分析设计空间。
8、对冰成核的精确控制
ControLyo技术
过冷程度是冷冻干燥放大的一大挑战。温度越低,过冷的程度就越高,导致冰晶变小。这会影响升华率和产品温度分布,导致实验室生成周期和商业制造生成周期之间的性能差异。冷冻是一个随机过程,冻干机内的小瓶在不同时间随机发生成核,产生异质批次和药品耐药性的可变性。
ATS SP Scientific的ControLyo技术利用惰性气体和一系列增压和减压步骤,实现在较高温度下控制所有小瓶瞬时成核。这将极大限度地减少过冷,并产生尽可能大的冰晶。当冰升华时,大晶体产生更大的空腔,使内部区域后续干燥的阻力更小,潜在干燥时间短,最终产品更容易复水。研究表明,成核温度每升高1℃,一次干燥时间减少3%。在某些情况下,ControLyo已被证明可以将周期时间从7.5缩短到5.5天,提高了生产率并提供了经济效益。

图5:ControLyo技术精确控制冰成核
许多新型生物药物的配方复杂,蛋白质含量高,灌装量大,在冷冻干燥时面临着很大的挑战。使用ControLyo可以确保较低的产品阻力,并提高批内与批间产品的均一性。因此,能为产品提供更积极的周期,扩大设计空间。ControLyo的另一个优点是,它可以安装或改装到任何冷冻干燥机上。
9、只需7个小瓶—加速冻干工艺开发
由于生物制剂的活性药物成分(API)价格昂贵,可用于冷冻干燥开发和优化的数量有限。LoS技术套件内的冷冻干燥机包括一个微型冻干机Lyoccapsule(图6),配备了创新的PAT工具和技术,且与SP其它更大规模的冻干机保持一致性。
Lyoccapsule只需7个小瓶,使用的材料更少,资源和准备时间也更少。这使得筛选更多的配方和优化干燥条件成为可能,远比在大型冷冻干燥机中更好。大一点规模的研发型及中试放大型冻干机,如LyoStar 4.0或 LyoConstellation,有助于进一步的工艺开发、优化、实验室规模的稳定性研究和放大。LyoConstellation冻干机的范围可以进一步用于从几百到几千瓶的批次的全面商业化生产。

图6:LyoCapsule: 7瓶微型研发型冻干机
10、从早期开发到商业化的平稳过渡
无论是在早期开发阶段、临床阶段、中试批次还是商业化生产阶段,有效生产高质量产品的关键参数都是相同的。然而,由于每个阶段设备之间的差异,从一个阶段转移到另一个阶段通常需要反复优化。
LoS技术套件由产品开发的每个阶段(Lyoccapsule, LyoStar 3, LyoConstellation)的冻干机组成,旨在通过在每个冻干机中提供经过验证的技术(SMART, LyoFlux TDLAS, Tempris和ControLyo)的连续性来尽可能大限度地减少这些差异。这种方法在每个阶段对结果进行了有意义的比较。
一些生物技术和制药公司已经认识到LoS对放大产品冻干过程的重要性。一家生物技术公司的一位科学家曾报告说:“Lyoccapsule可以用更少的API测试更多的条件,从而限制了财务风险。在产品开发的放大过程中使用相同的技术可以提供对产品更全面的理解,并且比传统的试错方法增加了成功的可能性。
11、结论
人类生长激素、胰岛素和红细胞刺激剂等生物制剂的开发,为新的治疗方式和生物疗法开辟了道路,这些药物可以用于对抗许多以前无法治愈的疾病。随着临床阶段的评估,许多分子的市场规模呈指数级增长。由于其复杂性和特点,生物制品的开发、制造和分销面临着许多挑战。通过冻干来稳定药物被认为是保持药物产品的生物活性、结构完整性和均一性的理想方法。
SP Line of Sight™
在明确的设计空间内开发和制造的QbD方法被认为是理想的实践之一,任何监管机构都期望采用。从对产品和条件的准确监测到整个冷冻干燥过程,ATS SP Line of Sight™工具套件支持QbD,以改进开发过程并保障生产的成功。LoS的设备设计和整合技术增加了操作空间的灵活性,提高了批量一致性,产量和产品质量。

图5:SP Line of Sight (LoS)
此外,该行业对冻干工艺的关键工艺参数和产品质量的非侵入式测量越来越感兴趣。这是由自动化的兴起推动的,因为 FDA要求将人员从流程中移除,以保护产品免受操作人员的伤害,以及开发高效配方以保护操作人员免受产品的影响。
LoS的一系列冷冻干燥器和创新技术使冻干条件在产品开发的早期阶段得到优化,提供产品知识,然后顺利转移到临床和生产阶段,而无需在每个阶段进行昂贵的重新优化。通过灵敏和无菌的监测装置和已建立的技术,可以准确、非侵入式地测量关键的冻干产品参数,提供一个丰富的数据环境。
这里的证据证明了优质生物药品生产设施所能获得的价值。通过投资ATS SP全套放大化技术,产品可以更有效地通过不同的开发阶段走向商业化。这些技术为持续理解受过程变量影响的质量属性提供了相同水平的产品和过程知识。这些努力简化了开发过程并建立了一致的产品质量,以降低长期经济负担并支持更佳患者治疗效果。

12、莱奥德创冻干课程
关注“莱奥德创冻干工场“,立即获取冻干讲堂的线上培训课程。
基于对于冻干研发的一些考量,莱奥德创创建了金字塔冻干培训平台:包含了从冻干理论基础,到配方和工艺开发,再到放大及生产,以及进阶的设备管理和线上线下专题培训课程。
课程结合了来自Biopharma的冻干理论培训课程体系、来自于莱奥德创产品经理及应用工程师的实践经验总结及国内外专家的专题培训内容。
课程获取方式
Step 1:关注公众号

扫码关注莱奥德创公众号
Step 2:点击菜单栏“冻干讲堂”
Step 3:点击你感兴趣的课程Banner
Step 4:开始学习