在 2024 年 12 月 18 日,美国食品药品监督管理局(FDA)正式批准了由 Mesoblast 公司生产的 remestemcel - L - rknd(商品名:Ryoncil)。这款疗法意义非凡,它属于异基因骨髓来源的间充质基质细胞(MSC)疗法,专门应用于治疗 2 个月及以上儿童患者所患的类固醇难治性急性移植物抗宿主病(SR - aGVHD)。值得一提的是,Ryoncil 成功摘得shou个获得 FDA 批准的 MSC 疗法的桂冠,这一突破性的成果无疑为相关疾病的治疗领域注入了全新的活力与希望,也将在医药研发历程中留下浓墨重彩的一笔,为后续更多细胞疗法的研发、审批及应用树立了典fan,开启了细胞疗法在临床应用上的新纪元,有望为众多饱受 SR - aGVHD 困扰的儿童患者及其家庭带来新的曙光与转机,推动整个医疗行业在难治性疾病治疗方面迈向新的台阶。
Ryoncil(remestemcel - L)是一种在生物医学领域具有重要意义的药物。它属于免疫调节剂,其独te之处在于它是由无关白细胞抗原(HLA)不匹配的健康成年供体的骨髓中提取的人间充质干细胞(hMSCs)制成。这些人间充质干细胞具备强大的免疫调节能力,能够抑制同种异体 T 淋巴细胞的增殖活性,在人体免疫反应的复杂网络中起到关键的调控作用。同时,在炎症反应过程中,Ryoncil 可有效减少促炎细胞因子的产生,从而减轻炎症对机体组织的损伤,为多种疾病的治疗带来了新的思路与希望
一波三折的审批历程
2008 年:开始使用当前经 FDA 检查的工艺制造改进版的 Ryoncil 产品.
2015-2018 年:进行了 3 期试验 MSB-GVHD 001 ,但因该试验中使用的 Ryoncil 产品缺乏合适的效力测定,其未被视为足以证明有效性的充分研究.
2020 年,美国食品药品监督管理局(FDA)的肿瘤药物咨询委员会(ODAC)以 9:1 的投票结果支持 Ryoncil 用于治疗儿童类固醇难治性急性移植物抗宿主病,但 FDA 最终未批准其上市,要求 Mesoblast 公司提供更多数据,并解决 Ryoncil 在化学、生产和质量控制方面的问题1.
此后,Mesoblast 公司提交了更新的临床数据,包括针对高风险儿童群体的匹配性研究以及 51 名儿童患者在 3 期试验中的 4 年存活数据等,但再次申请上市仍未获成功.
2023 年 9 月:Mesoblast 与美国食品药品监督管理局(FDA)举行了 A 型会议,FDA 明确了儿科批准的关键剩余问题是提供进一步证据,证明效力测定将确保商业产品的一致疗效。Mesoblast 打算在接下来的几个月内生成新的效力测定数据.
2024 年:Mesoblast 向 FDA 重新提交了 Ryoncil 的生物制品许可申请(BLA),并于 12 月 18 日获得 FDA 批准,成为美国首ge获批的间充质基质细胞疗法,用于治疗 2 个月及以上患有类固醇难治性急性移植物抗宿主病的儿科患者.
Ryoncil 的获批不仅是 Mesoblast 公司多年研发努力的结晶,更是全球生物医学领域在细胞治疗方向上的重大里程碑。它为那些深陷类固醇难治性急性移植物抗宿主病困境的儿童及其家庭带来了切实的希望之光。未来,随着对 Ryoncil 研究的持续深入以及相关临床应用经验的不断积累,相信其在治疗效果优化、适用范围拓展等方面将展现出更大的潜力,有望yin领更多创新细胞疗法的涌现,推动整个医疗行业向着攻克更多疑难病症的目标奋勇前行,为人类健康事业描绘出更为绚丽的蓝图,让我们拭目以待其在医学长河中续写辉煌篇章,持续为生命的守护与健康的恢复贡献卓yue力量。
逐典生物携手埃泽思生物,致力于提供MSCs全流程培养解决方案,从细胞源头起,贯穿始终,为您MSCs药物全流程开发保驾护航!
逐典相关产品推荐
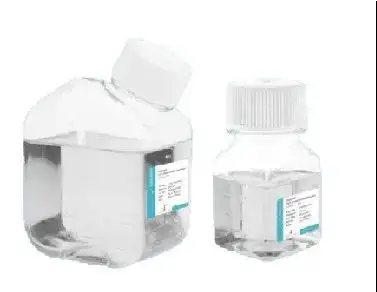
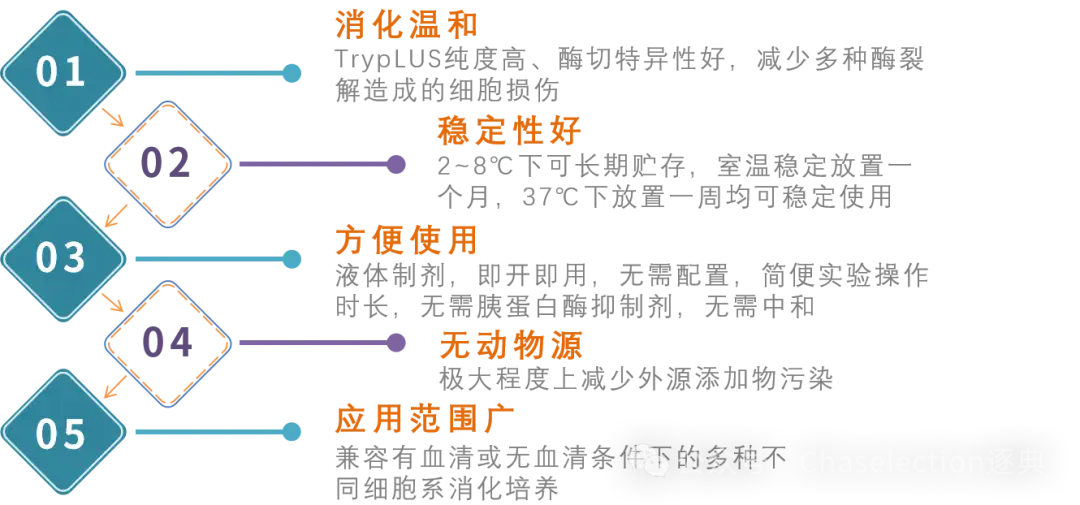
01Tryplus消化液
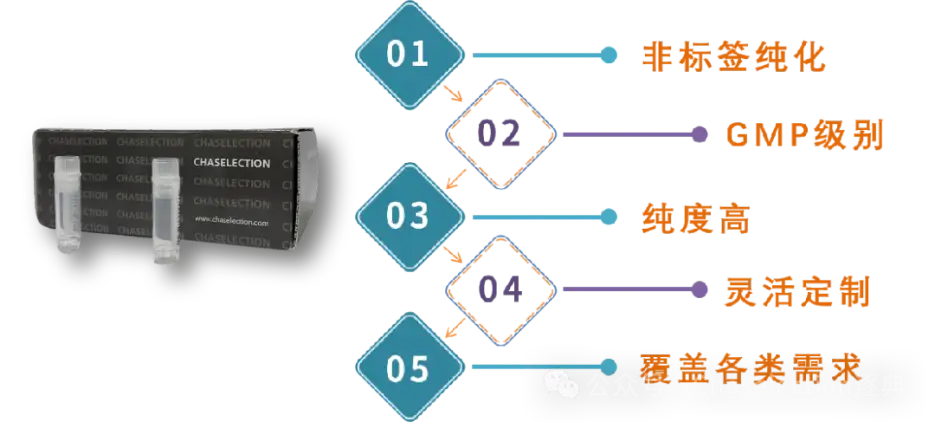
02细胞因子/改良型细胞因子
逐典相关产品订购信息

埃泽思相关产品推荐
01培养基
增强型人间充质干细胞培养基
AC-1001009

产品特点:
1、高效增殖能力,明显降低单位细胞生产成本;
2、传代稳定性高,最高可传20代细胞依然保持良好的形态和分化能力;
3、无动物源,成分确定,可以明显减少批间差异,确保每一批次产品的高效能和 稳定性;
4、符合细胞药物研发标准,可以进行药物研发申报;
人脐带间充质干细胞无血清培养基(无酚红)
AC-1001043PRF

产品特点
1、专为脐带间充质干细胞分离与扩增优化,传代稳定性高,最高可达20代;
2、全程无血清生产,极大降低批次间差异;
3、可用于原代分离,且培养过程无需包被培养板;
4、无外源动物成分,大大降低各类病毒、霉菌和支原体等的污染风险;
5、低热源,内毒素水平<0.12EU/mL
人脂肪干细胞无血清培养基(无酚红)
AC-1001042PRF

产品特点
1、专为脂肪间充质干细胞分离与扩增优化,传代稳定性高,最高可达20代;
2、全程无血清生产,极大降低批次间差异;
3、可用于原代分离,且培养过程无需包被培养板;
4、无外源动物成分,降低各类病毒、霉菌和支原体等的污染风险;
5、低热源,内毒素水平<0.12EU/mL
02定向分化试剂盒
人间充质干细胞成骨分化试剂盒
AC-1001027

产品特点
1、诱导分化程序简单便捷;
2、诱导成骨细胞效率高;
人间充质干细胞成软骨分化试剂盒
AC-1001028

产品特点
1、诱导分化程序简单便捷;
2、诱导成软骨细胞效率高;
人间充质干细胞成脂分化试剂盒
AC-1001029
产品特点
1、诱导分化程序简单便捷;
2、诱导成脂细胞效率高;
埃泽思相关产品订购信息

【关于逐典】
上海逐典生物科技有限公司,坐落于中国(上海)自由贸易试验区,获得ISO9001质量体系认证,是一家从事重组蛋白研发和销售的高新科技企业。
逐典生物始终秉持以客户为中心的理念,针对重组蛋白的结构设计、纯化工艺及其稳定剂型相关的多项关键技术进行优化和突破。专业的定向蛋白变复性技术,可将大肠杆菌大量表达的变性固体蛋白转变成高活性可溶性蛋白。凭借技术优势,逐典生物新品研发周期短且可控性强,为重组蛋白的高质高效研发提供保障,为企业生产降本增效。
公司自成立以来成功开发30余种高活性细胞因子及多种高活性蛋白酶,覆盖细胞培养、病毒纯化以及质量分析等生物工艺各个环节。可广泛应用于科研、医药生产及IVD(体外诊断试剂)等领域,满足各类用户所需。
【关于埃泽思】
埃泽思生物总部位于上海,公司取名Applied Cell (应用细胞),是一家致力于为细胞治疗、再生医学提供核心原料,以及研发服务(AA CRO) 和细胞药委托开发生产服务(CDMO)的生物科技公司。目前公司产品已经涵盖干细胞、免疫细胞治疗全流程试剂原料。其中核心产品已经完成美国FDA DMF备案以及国家药品评审中心(CDE)药物原辅料备案,是国内资质较为齐全的细胞治疗原料供应商。目前,公司已与国内多家细胞治疗企业进行细胞治疗一类新药联合申报。
