其他品牌 品牌
代理商厂商性质
北京市所在地
探测人体细胞产生的机械力装置
背景:
细胞具有产生力的能力,细胞使用物理力量来执行重要的功能——当这种力量被破坏时,在执行重要功能时缩短和再延长,疾病就会随之而来。传统上,测量这样的力是困难的,但是以下两种新的方法现在可以同时测量成千上万个细胞的细胞产生的力。
测试方案:
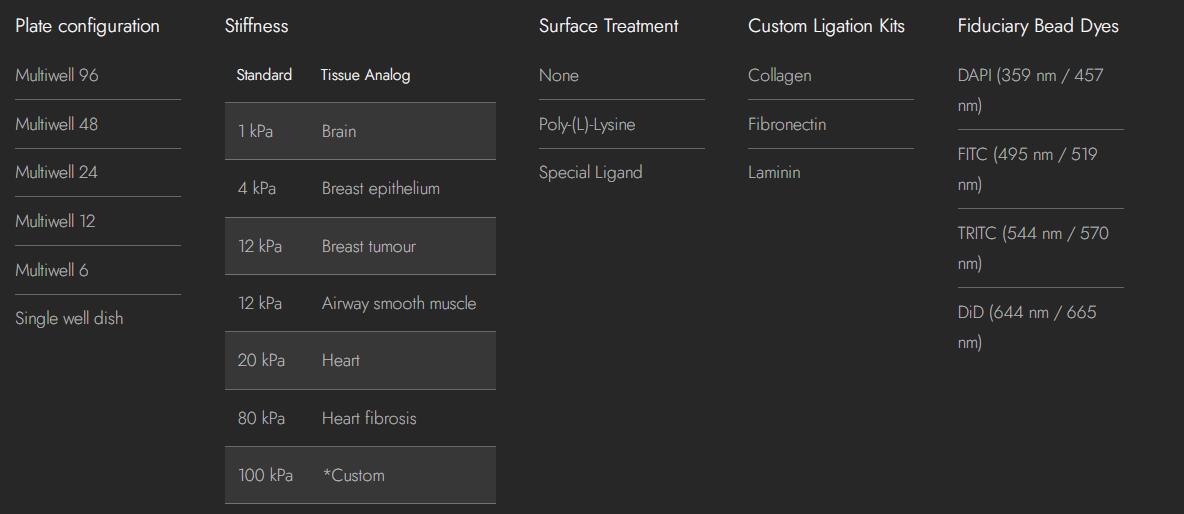
一、细胞收缩力高通量检测多孔板-24、96、384孔板:
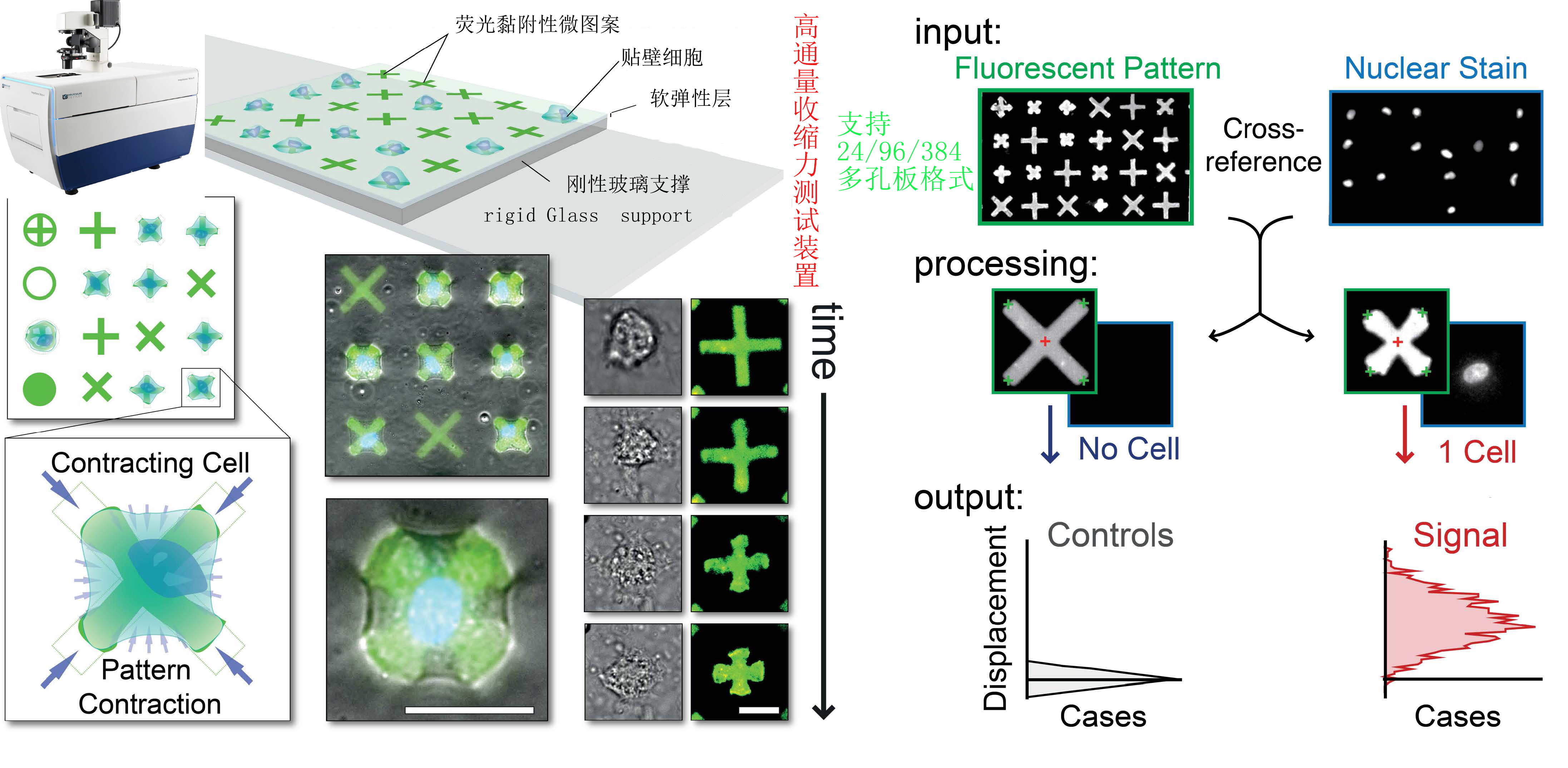
图1:原理图:
1.1)细胞收缩力测试24孔板
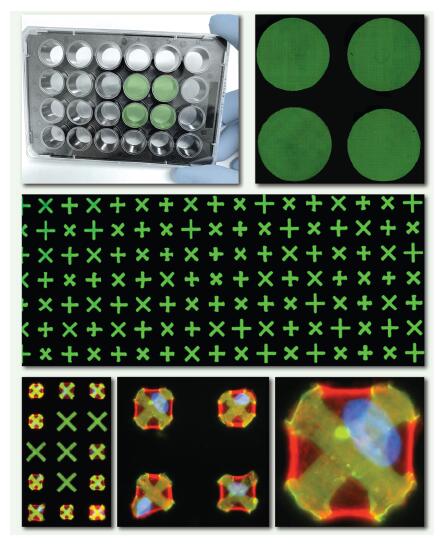
1.2)细胞收缩力测试384孔板
1.3)细胞收缩力测试384孔板

该可高通量检测细胞收缩力的多孔板是软膜底嵌有荧光微图案的*微孔板,上面有100,000多个均匀分布的X或+形的具有粘性蛋白质微图案,细胞沉降并附着在其上,嵌入板中的X具有弹性,因此每当细胞收缩时它们就会收缩。 X带有分子标记,可以发出荧光,从而可以成像和量化缩小的形状。
可以成像和定量,因此研究人员可以将X或十字架的变形与单个细胞或成千上万个细胞的一定量的力相关联。该技术还为研究人员提供了查看单个细胞钙反应以及它们与细胞强度之间的关系的能力。
该技术也可以用于药物发现。研究人员可以快速,轻松地测试不同的治疗分子,以了解它们如何影响细胞力以及是否可以纠正任何潜在的力问题。
在具有可控刚度的弹性薄膜中嵌入用户设计的粘合剂和荧光微图案,形成非常密集但均匀的阵列(> 120微米/每平方毫米)。100000个患者来源的单细胞(地从疾病起源的人体组织中获得)独立地定位并粘附在微图案上(每个微图案一个细胞),它们对该微图案施加牵引力并明显改变其形状,从而能够在*的吞吐量下对细胞收缩性进行直观的基于图像的评估。
1)荧光弹性可收缩表面的微图案化
—在具有可控刚度的弹性薄膜中嵌入用户设计的粘合剂和荧光微图案,形成非常密集但均匀的阵列(> 120微米/每平方毫米)。100000个患者来源的单细胞(地从疾病起源的人体组织中获得)独立地定位并粘附在微图案上(每个微图案一个细胞),它们对该微图案施加牵引力并明显改变其形状,从而能够在*的吞吐量下对细胞收缩性进行直观的基于图像的评估。
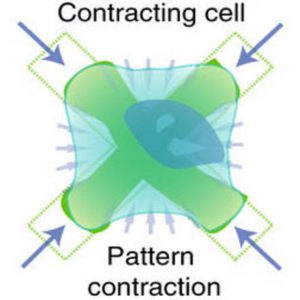
2)基于图像的受控单细胞收缩性的动力学可视化
—例如,384孔板内的每个附着细胞的微图案在延长的时间内以精细的时间分辨率被独立监控,以直接观察收缩行为的全部范围,从紧张性收缩到诱导性收缩或松弛,以及任一效应的作用窗口。选择“x”形微图案以小化细胞-基底接触面积,同时大化细胞扩散面积,从而在不同位置产生放大和集中的力。由于每个微图案都与其他微图案机械分离,粘附的细胞不会将应变传递给相邻的微图案,从而确保对群体中每个单个细胞的收缩力进行可靠的评估。
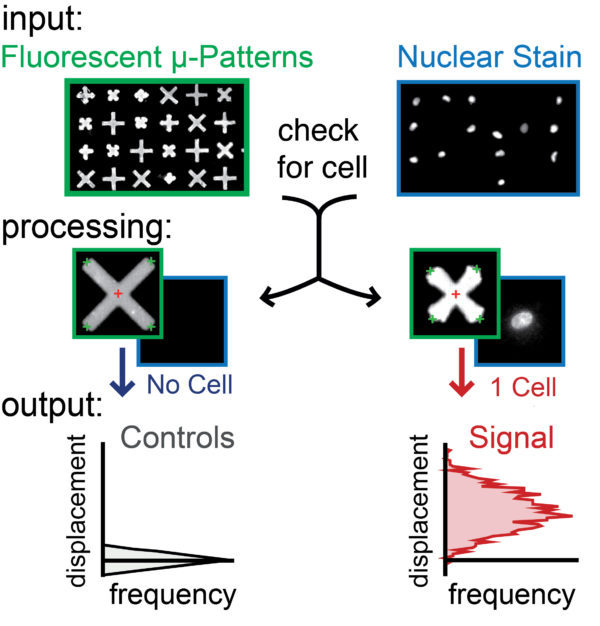
3)单细胞收缩性的自动化和直观的图像分析
—基于该方法的检测产生直观、明确的收缩信号——提供直接的图像分析,以从成像群体中的每个单细胞获得定量和可靠的数据。
可以同时获取1000多个均匀图案的单细胞的强大的收缩性数据,并与96-和384孔板格式无缝地集成,以促进大规模的药物筛选
二、细胞牵引力显微镜及微柱阵列介绍

图4:细胞牵引力显微镜

图5:细胞微柱阵列,可定制刚度、大小、形状和间距。
世联博研专注细胞力学、微观组织材料力学设备销售,提供细胞应力加载培养、微观力学测试分析系统等设备,点击此处查看更多

在生理和病理条件下,细胞本身产生的或细胞外基质 (ECM) 通过粘着斑 (FA) 和粘附连接 (AJ) 传递的机械力已知在调节各种细胞行为中发挥重要作用。
细胞胞力的产生和力的传递:
对于许多生物过程至关重要,量化通过基于E-钙粘蛋白的粘附连接施加的细胞-细胞和细胞内力,将在生物学研究领域阐明与机械力响应相关的细胞功能方面发挥基础性作用,
该系统为理解生物力学力在单个细胞、多细胞以及细胞-细胞/细胞-ECM 界面上的作用的提供了新方法,将为革新再生医学、疾病建模和药物发现的突破性技术打开大门,
阐明了细胞迁移、增殖、分化、重塑和机械感知其微环境的机制的许多方面。
该系统支持基于微柱阵列法、FLECS荧光弹性基底微图案法、集成荧光微珠嵌入聚丙烯酰胺凝胶法、PDMS合规的薄硅膜法,集优弃劣进行力生成和应力传递分析,可以2D细 胞,也可以3D细胞嵌入水凝胶中,并结合时间依赖性 (4D)的细胞内源力产生与力传递量化分析实验。可用于单个细胞、多细胞之间、细胞集落和融合细胞层(cell sheet)中的力生成和应力传递分析,为理解生物力在单个细胞、细胞集落、细胞-细胞/细胞-ECM界面上的作用提供了新方法,将为革新再生医学、疾病建模和药物发现的突破性技术打 开大门,阐明了细胞迁移、增殖、分化、重塑和机械感知其微环境的机制的许多方面,对于深刻理解许多生物过程至关重要。
该系统解决了从具有已知弹性的粘性基底测量的细胞力引起的变形重建细胞基质牵引力和细胞间和细胞内应力的逆问题。除了应力和力生成的标准测量之外,
还可以进行包括线性张力测量(一种专门用于细胞边界的力传递测量),允许用户设置所必要的分析参数,选择感兴趣的区域,检查输入参数和中间结果,
并计算描述力、应力及其分布的各种参数,允许非用户对此类实验进行全面评估,可让您快速分析可视化大型数据集。
可选配时差显微镜活细胞工作站,为显微镜提供类似培养箱的气体温度湿度控制;
可选的共聚焦超高分辨率TIRF显微镜
2.2.1、细胞微柱阵列:
细胞主要黏附于与基底垂直微柱的上面,可以直接根据微柱的弯曲变形程度与方向测定与细胞接触点牵引力的大小与方向。
2.2.2、荧光微珠嵌入聚丙烯酰胺凝胶:
通过培养在具已知弹性软基底(聚丙烯酰胺(PA)胶),细胞收缩过程中对基底产生的牵引力使基底产生变形,这种变形反映到荧光微珠的运动;用荧光显微镜采集荧光微珠的运动信息,经图像处理后,得到基底的应变信息,然后通过一定的力学模型,定量反演出细胞的牵引力;细胞收缩或迁移过程中各个时刻的力分布就可以可视化在计算机屏幕上
2.2.3、荧光弹性可收缩表面微图案化多孔板高通量细胞收缩力检测多孔板-24、96、384孔板:
该可高通量检测细胞收缩力的多孔板是软膜底嵌有荧光微图案的du特微孔板,上面有100,000多个均匀分布的X或+形的具有粘性蛋白质微图案,细胞沉降并附着在其上,嵌入板中的X具有弹性,因此每当细胞收缩时它们就会收缩。 X带有分子标记,可以发出荧光,从而可以成像和量化缩小的形状
2.2.4、合规PMDS基底多孔板:
采用软弹性基底,通过细胞与弹性基底相互作用引起的基底变形来测定或计算细胞牵引力
可定制刚度0.1kPa 至 100 kPa 的杨氏弹性模量、蛋白质涂层
2D单个细胞、3D凝胶包埋的细胞、细胞集落和融合细胞层中的力生成和应力分析,细胞收缩力、细胞之间相互用力、细胞与ECM之间相互用力、跨细胞边界作用力、平均法向应力和剪切应力
有许多不同的方法可以测量力的产生和应力。在这里,您可以找到可以使用该程序计算的数量的概览。
zui简单的方法是总结细胞附着的基底表面的变形。变形取决于基材的机械性能。

收缩力定义为牵引力向一个点(称为力中心)的投影之和。因此,如果力都已经指向一个中心点,则收缩性很高。局部相反的力和不指向力震中的力对收缩性没有贡献。能够以力似乎源自单个点的方式协调其力产生的细胞或细胞群可以获得高收缩性,同时消耗相对少量的应变能。
这在图13中进一步说明。案例 A 代表具有两个具有高度协调力生成的细胞的细胞集落,案例 B 代表具有协调性的细胞。在情况 B 中,每个细胞自行产生收缩力。因此,如果我们假设情况 A 和 B 中的应变能相等,则情况 B 的收缩性较低。
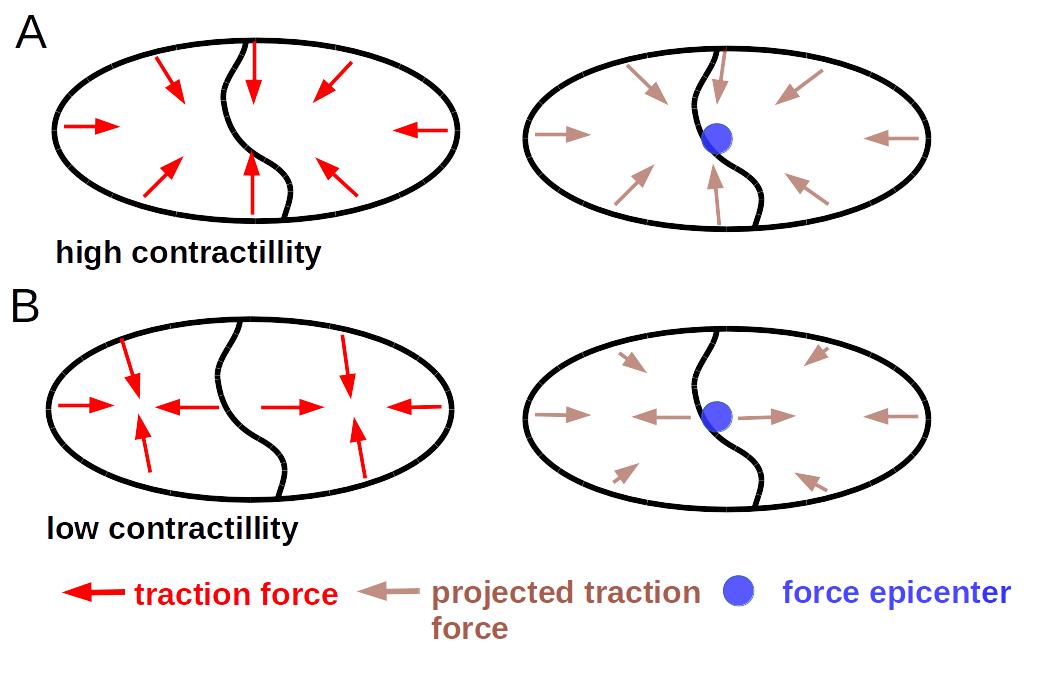
综上所述:应变能是总力产生的量度,而收缩性是协调力产生的量度。
压力描述了在细胞或细胞片内部传递的力。对于细胞表中的任何给定点,应力由具有 4 个分量的张量定义。如图 14所示,每个分量代表将作用于从细胞片切出的正方形边缘的力。
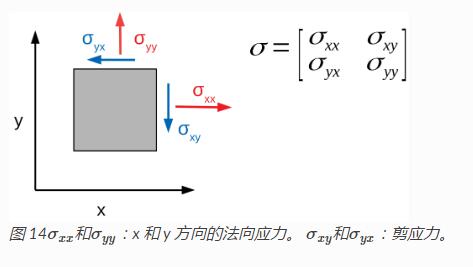
我们可以区分两种类型的应力:剪切应力,一种平行于该正方形边缘作用的力,以及法向应力,一种垂直于该正方形边缘作用的力。由于几何原因,应力张量的两个剪切分量必须相同。普通组件不是这种情况。由于法向应力是否主要来自 x 或 y 方向对我们的分析没有意义,因此计算两个分量的平均值更有用。这留下了两个应力:剪应力和平均法向应力。这些压力可以在整个细胞集落区域进行平均。
应力分布可以用变异系数 (CV) 来描述,即用平均法向应力或剪切应力的平均值归一化的标准偏差。
如上所述,应力张量可用于计算作用于细胞集落边界的力。这种力称为线张力,有一个直接的解释:想象一下,您实际上要沿着两个细胞之间的边界切割细胞片。如果细胞继续产生力,则该切口的边缘会漂移开或开始重叠,因为您刚刚切割了将两个边缘固定在一起的材料。为了将两个边缘保持在切割之前的位置,您需要在边缘施加一个力。这个力,由切割长度归一化,是线张力。
线张力是具有 x 和 y 分量的向量。与应力类似,它可以分为剪切分量(平行于切口作用的力)和法向分量(垂直于切口作用的力)。两者都有助于线张力的大小(线张力矢量的长度)。
使用该系统计算细胞间应力,以获得面内二维应力张量。简而言之,应用牛顿定律要求的直接力平衡,为我们提供单层内的二维应力张量,通过旋转单层内每个点的坐标系。此外,在单层内的每个点,我们计算了平均正常细胞间应力 (σ max + σ min )/2 和zui大剪切细胞间应力 (σ max -σ min )/2
我们的平台兼容2D/3D/4D模式,支持单细胞、融合单层细胞以及介于两者之间的细胞。可按需定制,包括孔格式、模量、珠荧光、玻璃厚度和分析软件的定制。我们可以提供任何组合,制造您想要的,并且乐于为您的挑战创新解决方案。